
技术文章
Technical articles 热门搜索:
促甲状腺激素受体人单克隆抗体 M22
甲状腺自免-TRAb ELISA试剂盒
RSR 乙酰胆碱受体抗体ELISA试剂盒
神经免疫-RSR 水通道蛋白4抗体ELISA试剂盒
糖尿病抗体ELISA检测试剂盒
RSR-水通道蛋白4抗体ELISA检测试剂盒
RSR 锌转运蛋白8 ZnT8抗体ELISA试剂盒
糖尿病自身免疫抗体(GAD+IA2)ELISA试剂盒
RSR谷氨酸脱羧酶抗体 GAD Ab ELISA试剂盒
RSR ELISA-IA-2抗体检测试剂盒
RSR ELISA-ZnT8Ab试剂盒
RSR-VGKC 抗体RIA检测试剂盒
猫、狗慢性肾病-DLD SDMA ELISA试剂盒
RSR-乙酰胆碱受体抗体AChRAb RIA试剂盒
RSR-VGCC 抗体RIA检测试剂盒
肾上腺自免-RSR 21-羟化酶抗体ELISA试剂盒
热门搜索:
促甲状腺激素受体人单克隆抗体 M22
甲状腺自免-TRAb ELISA试剂盒
RSR 乙酰胆碱受体抗体ELISA试剂盒
神经免疫-RSR 水通道蛋白4抗体ELISA试剂盒
糖尿病抗体ELISA检测试剂盒
RSR-水通道蛋白4抗体ELISA检测试剂盒
RSR 锌转运蛋白8 ZnT8抗体ELISA试剂盒
糖尿病自身免疫抗体(GAD+IA2)ELISA试剂盒
RSR谷氨酸脱羧酶抗体 GAD Ab ELISA试剂盒
RSR ELISA-IA-2抗体检测试剂盒
RSR ELISA-ZnT8Ab试剂盒
RSR-VGKC 抗体RIA检测试剂盒
猫、狗慢性肾病-DLD SDMA ELISA试剂盒
RSR-乙酰胆碱受体抗体AChRAb RIA试剂盒
RSR-VGCC 抗体RIA检测试剂盒
肾上腺自免-RSR 21-羟化酶抗体ELISA试剂盒
 更新时间:2021-11-29
更新时间:2021-11-29 点击次数:1666
点击次数:1666
天津医科大学朱宪彝纪念医院陈莉明教授团队在Acta Diabetologica上发表了一项新研究,是国内初次成功应用3-Screen ICA ELISA检测表型为2型糖尿病患者的糖尿病自身抗体。英国RSR和天津阿斯尔共同参与了这项研究。
编者按
虽然单项胰岛细胞自身抗体的检测具有很好的敏感性、特异性且标准化的操作,但并不适合用于大样本筛查,而3-Screen已被证明在大规模人群筛查和预测1型糖尿病(T1DM)中是一种有力工具。近日,天津医科大学朱宪彝纪念医院陈莉明教授团队在Acta Diabetologica上发表了一项新研究,是国内初次成功应用3-Screen ICA™ ELISA检测表型为2型糖尿病(T2DM)患者的糖尿病自身抗体。下面,我们一起来看看这项研究。

要点概览
利用3-Screen检测方法在中国成人T2DM患者中鉴定出3.5%(44/1273)的患者呈糖尿病自身抗体阳性(归类为LADA)。
3-Screen阳性患者相对于典型的T2DM具有LADA“三低一高"的特征:更低的BMI、更低的空腹胰岛素和C肽水平,更高的HbA1c水平。同时有更高的DKA风险和/或胰岛素治疗需求。
3-Screen阳性患者有发生相关自身免疫疾病的风险,特别是自身免疫性甲状腺疾病。
3-Screen检测将助力LADA患者的临床诊断,减少卫生服务负担。
3-Screen ICA™ ELISA检测试剂盒具有方便、经济且一步式的特点,适用于大量样本的筛查。

引言
成人隐匿性自身免疫糖尿病(LADA)是一种缓慢起病的自身免疫糖尿病。对其在糖尿病中的分型研究,经历过以下几个阶段:① 1999年WHO对糖尿病进行分型时,将LADA归类于自身免疫介导T1DM的缓慢进展亚型;② 2019年WHO分型更新,将LADA和酮症倾向的T2DM归类于混合型糖尿病;③ 2020年ADA指南指出,LADA存在自身免疫β细胞破坏,属于T1DM。LADA临床表型虽与T2DM重叠,但病理机制与T1DM相似,均为胰岛自身免疫[1]。
根据2015年发表的全国多中心的LADA China研究报道,使用单一谷氨酸脱羧酶抗体(GADAb)筛查,在新发T2DM患者中LADA患病率达5.78%;联合GADAb、蛋白酪氨酸磷酸酶抗体(IA-2Ab)和锌转运体-8抗体(ZnT8Ab)等多抗体筛查,LADA患病率为8.63%[2]。此外,ADOPT研究报告称,北美新发确诊T2DM患者中GADAb阳性率为4.7%,欧洲为3.7%[3]。
虽然单项胰岛细胞自身抗体(GADAb、IA-2Ab和ZnT8Ab)的检测具有很好的敏感性、特异性且标准化的操作[4-6],但由于成本和检测时间的原因,不适合用于大量样本的筛选。3-Screen是一种新型的ELISA检测方法,可联合检测血清中GAD、IA-2和ZnT8三种抗体,且单项自身抗体的检测结果与3-Screen的检测结果一致[7]。3-Screen已被证明在大规模人群筛查和预测T1DM中是一种有力工具。例如,在T1DM Fr1da研究中,90 632例巴伐利亚儿童最初采用3-Screen筛查,其中280例(0.31%)发现多种β细胞自身抗体阳性[8]。
陈莉明教授团队使用新型3-Screen ICA™ ELISA(3-Screen)试剂盒联合检测单个血清样本中的GADAb、IA-2Ab和ZnT8Ab,旨在评估糖尿病相关自身抗体在新近确诊为成年发病型T2DM的中国患者中的检出率,并评估自身抗体标志物对表征疾病表型的潜在价值,尤其是在3-Screen阳性患者与3-Screen阴性患者的临床特征和代谢谱方面。3-Screen检测的辅助和特征性疾病表型的识别,有助于为具有糖尿病自身抗体的成人T2DM患者及时正确地量身定制治疗方案。
材料和方法
01
患者
一项基于医院的横向研究在中国天津医科大学朱宪彝纪念医院进行。2014年4月~2016年10月,1273例诊断为T2DM表型的患者根据特定标准被纳入研究:(a)≥18岁患者空腹血糖≥7.0 mmol/L、餐后及随机血糖≥11.1 mmol/L诊断为糖尿病;(b)病程<1年;(c)诊断糖尿病后6个月内无糖尿病酮症酸中毒(DKA)。所有1273例T2DM表型患者被分配到不同的治疗方案,包括口服糖尿病药物或胰岛素治疗,或如果患者不能通过饮食和运动维持目标血糖水平,则两者联合。
02
抗体检测
对该研究中1273例患者血清样本使用3-Screen ICA™ ELISA检测自身抗体。所有3-Screen(>10 U/ml)阳性患者均采用RSR公司提供的单项ELISA法检测GADAb、IA-2Ab和ZnT8Ab。所有3-Screen阳性样本也检测了其他器官特异性自身抗体,包括促甲状腺激素受体(TSHR)抗体、甲状腺过氧化物酶(TPO)抗体、甲状腺球蛋白(Tg)抗体和类固醇21-羟化酶(21-OH)抗体。
结果
01
T2DM患者中糖尿病相关自身抗体的
检出率为3.5%
在研究的1273例T2DM患者中,有44例(3.5%)3-Screen阳性。而在这44例患者的单项自身抗体检测中,GADAb阳性者35例(80%),IA-2Ab阳性者5例(11%),ZnT8Ab阳性者12例(27%)。6例3-Screen阳性样本在单项抗体ELISA试剂盒检测中为阴性(图1)。
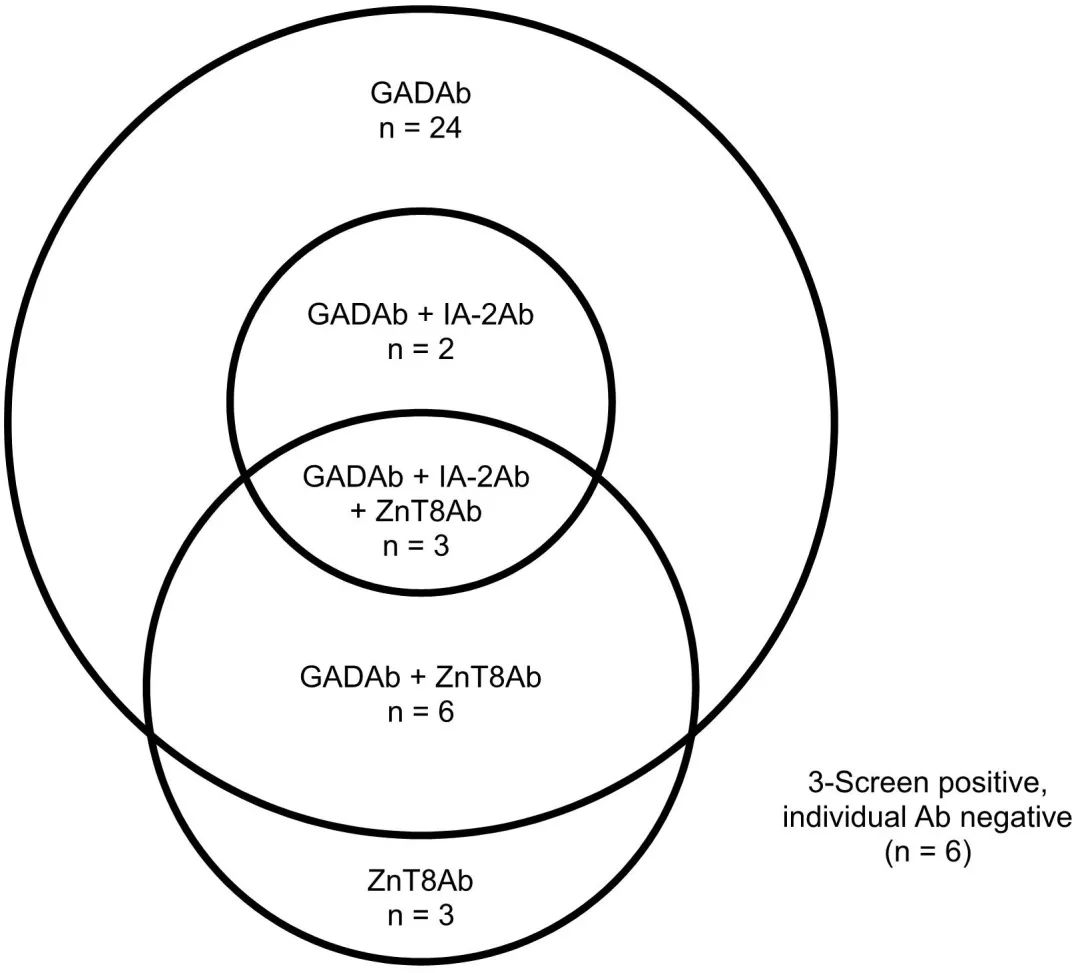
图1. 44例3-Screen ICA™ ELISA阳性(>10 U/ml)患者GADAb、IA-2Ab和ZnT8Ab的维恩图
02
3-Screen阳性的T2DM患者
无显著的年龄特征差异
结果显示,不同年龄组间3-Screen阳性率无显著差异(P=0.06,图2)。

图2. 3-Screen阳性的T2DM患者的年龄差异
03
3-Screen阳性的T2DM患者
具有显著的临床特征
表1. T2DM表型患者3-Screen阳性组和3-Screen阴性组的临床特征
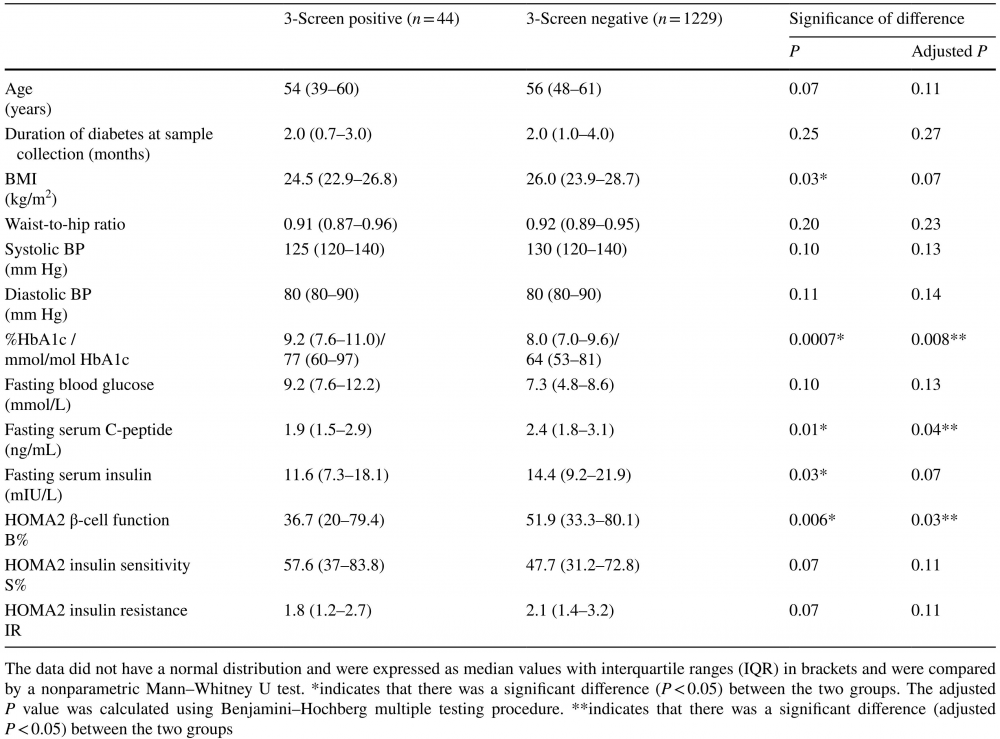
(点击查看大图)
表2. 3-Screen阳性患者是否伴有DKA和/或胰岛素治疗的特征(使用分类数据分析)
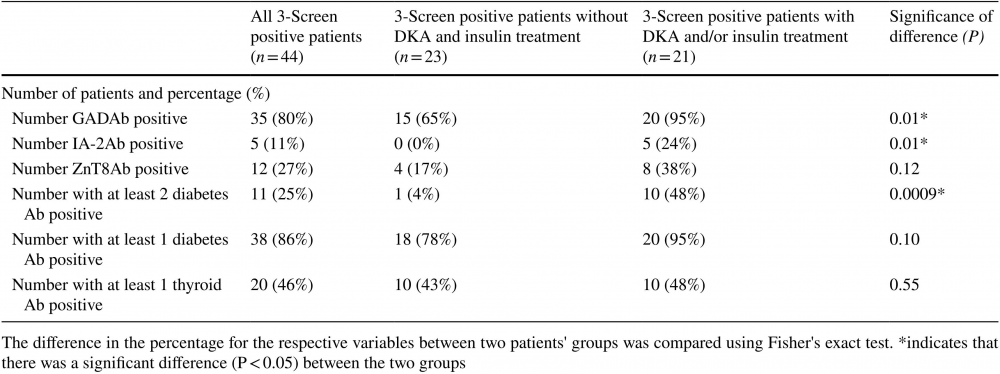
(点击查看大图)
04
LADA患者易伴发甲状腺自身免疫疾病
自身免疫性糖尿病与其他器官特异性自身免疫性疾病存在联系。表2中44例3-Screen阳性患者中,20例(46%)至少存在1种甲状腺自身抗体。而在该20例患者中,4例(20%)在功能指标上体现为甲状腺功能减退。与先前的观察结果一致,这提示胰岛细胞自身抗体阳性的成人糖尿病患者有发展为相关自身免疫疾病的风险,尤其体现在甲状腺自身免疫疾病上。
总结
3-Screen ICA™ ELISA可联合检测血清中GAD、IA-2和ZnT8三种糖尿病自身抗体。本研究中呈现3-Screen阳性的成人糖尿病患者表现出与胰岛β细胞功能低下相关的特征性临床表型。由此提示,该类患者在糖尿病确诊后的疾病管理中更应获得密切的健康监测,尤其是胰岛素治疗的需求。由于LADA在临床特征上存在高度异质性,在制定治疗方案方面,特别是延缓胰岛β细胞功能减退的针对性措施,需要对新发的非T1DM进行准确诊断和分型。在分型依据之一的自身抗体检测中,与传统的单项检测相比,联合检测具有方便、经济且一步式的特点,适合新发糖尿病患者的自身抗体大样本筛查。相信在将来的自身免疫糖尿病疾病诊疗中,3-Screen联合检测将会助力LADA患者的临床诊断,减少卫生服务负担。
专家简介

陈莉明
天津医科大学朱宪彝纪念医院
主任医师,教授,博士生导师
国务院特殊津贴专家,国家卫健委突出贡献专家
海河学者,天津名医,天津市高校人才
中华医学会糖尿病学分会副主任委员
中国微循环学会糖尿病与微循环学会副主任委员
天津糖尿病学会主任委员
国家自然科学基金评审人
《Diabetes Metabolism Research and reviews》《中华内分泌代谢杂志》《中华临床营养杂志》编委,《中华糖尿病杂志》副主编,《国际内分泌与代谢病杂志》主编
参考文献
1. 中国医师协会内分泌代谢科医师分会, 国家代谢性疾病临床医学研究中心. 成人隐匿性自身免疫糖尿病诊疗中国专家共识(2021版). 中华医学杂志. 2021; 101(38): 3077-3091.
2. Xiang Y, Huang G, Shan Z, et al. Glutamic acid decarboxylase autoantibodies are dominant but insufficient to identify most Chinese with adult-onset non-insulin requiring autoimmune diabetes: LADA China study 5. Acta Diabetol. 2015; 52(6): 1121-1127.
3. Zinman B, Kahn SE, Hafner SM, et al. Phenotypic characteristics of
GAD antibody-positive recently diagnosed patients with type 2 diabetes in North America and Europe. Diabetes. 2004; 53(12): 3193-3200.
4. Bingley PJ, Bonifacio E, Mueller PW. Diabetes Antibody Standardization Program: first assay proficiency evaluation. Diabetes. 2003; 52(5): 1128-1136.
5. Törn C, Mueller PW, Schlosser M, et al. Diabetes Antibody Standardization Program: evaluation of assays for autoantibodies to glutamic acid decarboxylase and islet antigen-2. Diabetologia. 2008; 51(5): 846-852.
6. Lampasona V, Schlosser M, Mueller PW, et al. Diabetes antibody standardization program: first proficiency evaluation of assays for autoantibodies to zinc transporter 8. Clin Chem. 2011; 57(12): 1693-1702.
7. Amoroso M, Achenbach P, Powell M, et al. 3 Screen islet cell autoantibody ELISA: A sensitive and specific ELISA for the combined measurement of autoantibodies to GAD65, to IA-2 and to ZnT8. Clin Chim Acta. 2016; 462: 60-64.
8. Ziegler AG, Kick K, Bonifacio E, et al. Yield of a Public Health Screening of Children for Islet Autoantibodies in Bavaria, Germany. JAMA. 2020; 323(4): 339-351.
更多关于自身免疫性疾病相关抗体的资料:请详见产品列表。